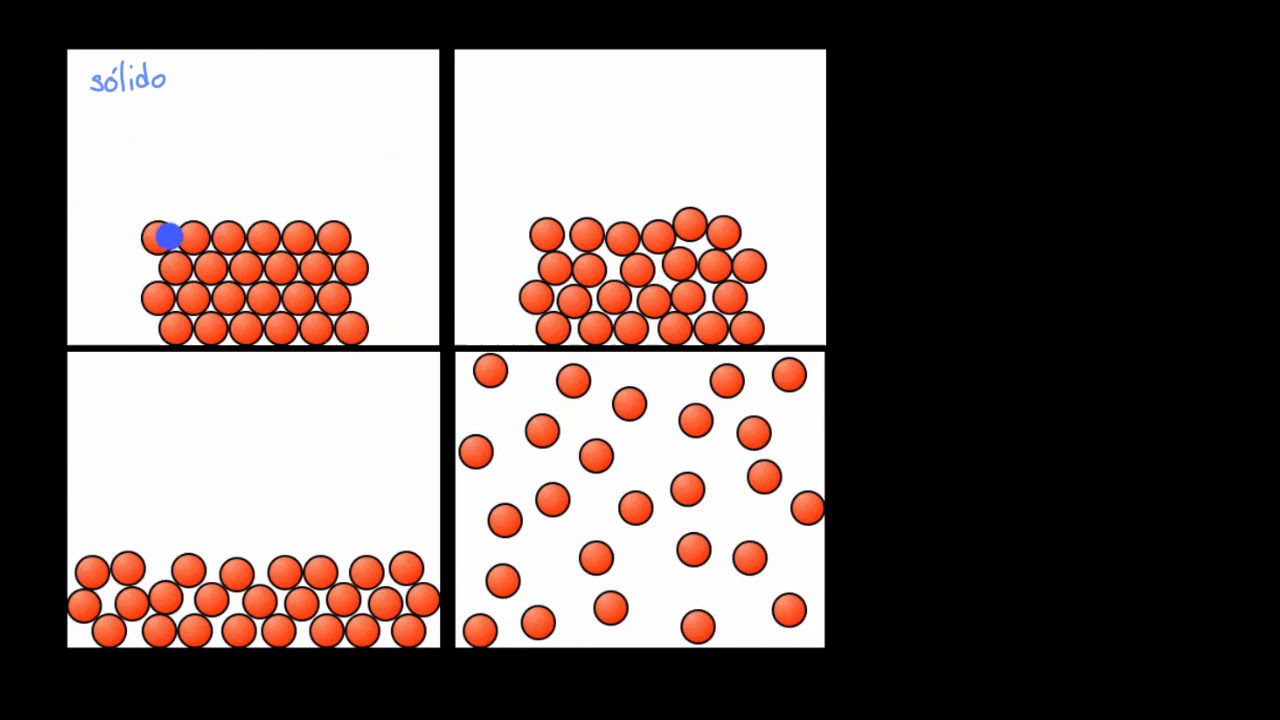
Entender los estados de la materia y su comportamiento a nivel molecular.
¿Qué es el modelo de partículas?
Cuando hablamos del modelo de partículas, nos referimos a una forma intuitiva de entender cómo está constituida la materia. Cada pequeño componente de un material, ya sea un sólido, un líquido o un gas, está formado por partículas diminutas que interactúan entre sí. Imagina que estas partículas son como un grupo de amigos en una fiesta: su comportamiento cambia según el ambiente en el que se encuentren.
Los estados de la materia: Un pequeño vistazo
La materia puede encontrarse en tres estados principales: sólido, líquido y gaseoso. Cada uno de estos estados tiene sus propias características, que dependen del movimiento y las fuerzas de atracción entre las partículas. Veamos más a fondo cada uno de ellos.
Sólido: La rigidez estructural
En el estado sólido, las partículas están muy juntas y vibran en su lugar, como si estuvieran en una especie de baile estático. Esta interacción fuerte y cercana les da forma fija y un volumen bien definido. Piensa en un cubo de hielo: su forma no cambia sin importar dónde lo coloques, y eso es gracias a la organización compacta de sus moléculas.
Características de los sólidos
- Forma definida: Los sólidos tienen un contorno que no cambia fácilmente.
- Volumen constante: No ocuparán más o menos espacio sin ser alterados.
- Dureza variable: Dependiendo del material, pueden ser muy duros, como el diamante, o más suaves, como la cera.
Líquido: Fluyendo con gracia
Si observamos un líquido, como el agua, notaremos que las partículas están más separadas que en un sólido. A diferencia de los amigos en una fiesta, donde algunos se mueven más libremente, aquí las partículas se deslizan unas sobre otras. Esto permite que el líquido tome la forma del recipiente en el que se encuentra, manteniendo su volumen pero sin una forma fija.
Características de los líquidos
- Forma variable: Los líquidos adoptan la forma del recipiente que los contiene.
- Volumen constante: Aunque cambian de forma, su volumen permanece igual.
- Fluidez: Tienen la capacidad de moverse y fluir con facilidad.
Gaseoso: La libertad de las moléculas
En el estado gaseoso, las partículas están muy separadas y se mueven libremente. Imagina a esas personas en una fiesta donde hay demasiado espacio: pueden bailar y moverse como les plazca. Este comportamiento da lugar a que los gases no solo tomen la forma del recipiente, sino que también llenen todo el espacio disponible. Así que, si abres un refresco, ¡el gas se expandirá rápidamente!
Características de los gases
- Forma y volumen variables: Los gases no tienen una forma definida ni un volumen fijo; se expandirán hasta llenar cualquier espacio.
- Compatibilidad: Los gases pueden mezclarse fácilmente entre sí, como si fueran una gran mezcla de diferentes sabores.
- Baja densidad: Generalmente, los gases son menos densos que los líquidos y sólidos.
Transiciones entre estados: El baile de la materia
Ahora que entendemos las características de cada estado de la materia, es interesante hablar sobre las transiciones entre ellos. Estas ocurren debido a cambios en la temperatura y presión. Cada transición es como un baile que empieza a acelerarse o ralentizarse dependiendo del ritmo de la música (la energía). ¿Te suena?
Fusión: De sólido a líquido
Cuando un sólido absorbe suficiente calor, sus partículas comienzan a vibrar más rápido y se separan, convirtiéndose en un líquido. Este proceso se llama fusión. Piensa en un hielo que se derrite: ¡es una transformación mágica!
Evaporación: De líquido a gas
La evaporación es el proceso mediante el cual un líquido se convierte en gas. Cuando las partículas del líquido tienen suficiente energía para vencer la atracción entre ellas, se escapan a la atmósfera, como un caprichoso niño que decide correr libremente en el parque. ¡Justo así, el agua se convierte en vapor!
Condensación: De gas a líquido
La condensación es el camino contrario. Cuando el vapor se enfría, las partículas pierden energía, se acercan y formen gotas de agua, como cuando ves que el vapor de la ducha se convierte en pequeñas gotas en el espejo.
Solidificación: De líquido a sólido
La solidificación es el proceso en el cual un líquido se convierte en sólido al perder calor. Cuando el líquido se enfría lo suficiente, las partículas se organizan en un patrón fijo, como cuando haces helado en casa y lo metes en el congelador.
Sublimación: De sólido a gas
La sublimación es un proceso curioso en el cual un sólido se convierte directamente en gas sin pasar por el estado líquido. Un ejemplo clásico es el hielo seco, que se descompone en dióxido de carbono gaseoso. ¡Una verdadera magia científica!
Desublimación: De gas a sólido
Este fenómeno se da cuando un gas se convierte en sólido. Un ejemplo sereno es el de las escarchas que se forman en una helada de la noche, donde el vapor de agua en el aire se congela rápidamente.
Factores que afectan los estados de la materia
Los cambios en temperatura y presión son como luces en una pista de baile: pueden cambiar el ritmo de las partículas. Pero, ¿qué otros factores pueden modificar los estados de la materia?
Temperatura
Como ya mencionamos, la temperatura es fundamental. Cuando aumenta la temperatura, las partículas ganan energía y se mueven más rápido. Al bajarla, las partículas pierden energía y se acercan. ¡Es un juego constante!
Presión
La presión también desempeña un papel crucial. Incrementar la presión puede forzar a las partículas a disminuir su distancia y cambiar un gas a un líquido. Piensa en una lata de refresco: si aplicas suficiente presión, ¡el gas se convierte en líquido!
Composición del material
Los diferentes materiales tienen distintas interacciones entre sus partículas. Esto significa que algunos materiales necesitan más energía (calor) para cambiar de estado, mientras que otros lo hacen con más facilidad.
Importancia del modelo de partículas en la ciencia
El modelo de partículas no solo es fascinante, sino que también es esencial para entender muchos aspectos de la ciencia. Desde la química hasta la física, este modelo nos ayuda a predecir cómo se comportará la materia en diferentes condiciones. ¡Es como tener un mapa que nos guía en un mundo complejo!
Aplicaciones prácticas en la vida diaria
Entonces, ¿por qué deberías importar el modelo de partículas? Aquí algunos ejemplos prácticos:
Calentadores y refrigeradores
Los dispositivos que usamos todos los días, como los refrigeradores, funcionan según el principio de cambiar los estados de la materia. Entender cómo se comportan las partículas del refrigerante nos ayuda a mejorar la eficiencia energética.
Cocción de alimentos
El proceso de hervir agua para cocinar pasta o el uso de un sartén para freír son ejemplos de cómo aplicamos la conocimiento del modelo de partículas en la cocina. Estos métodos dependen del movimiento y la energía de las partículas en el agua o en los ingredientes.
¿Se pueden tener más de tres estados de la materia?
Sí, existen otros estados más allá de los tres comunes, como el plasma (en el cual las partículas están ionizadas) y los condensados de Bose-Einstein, que ocurren en condiciones extremadamente frías.
¿Qué sucede con las partículas a temperatura cero?
A cero absoluto, las partículas casi dejan de moverse por completo, esto se cree que es el límite más bajo de energía térmica.
¿Cómo se pueden observar los estados de la materia en la naturaleza?
Los estados de la materia se pueden observar en fenómenos naturales, como los océanos (líquido), montañas (sólido) y nubes (gas).
El modelo de partículas proporciona una base sólida para comprender la materia y sus reacciones. Al aprender cómo las partículas interactúan en diferentes estados, no solo enriquecemos nuestro conocimiento científico, sino que también mejoramos nuestra comprensión del mundo que nos rodea. ¿Listo para seguir explorando y descubriendo más sobre la magia de la materia?